
Química Geral
Assessment
•
Prof Diniz
•
Chemistry
•
1st Grade - University
•
17 plays
•
Hard
Improve your activity
Higher order questions
Match
•
Reorder
•
Categorization
.svg)
actions
Add similar questions
Add answer explanations
Translate quiz
Tag questions with standards
More options
20 questions
Show answers
1.
Multiple Choice
No texto: “Um escultor recebe um bloco retangular de mármore e, habilmente, o transforma na estátua de uma celebridade do cinema”, podemos identificar matéria, corpo e objeto e, a partir daí, definir esses três conceitos.
I. Matéria (mármore): tudo aquilo que tem massa e ocupa lugar no espaço.
II. Corpo (bloco retangular de mármore): porção limitada de matéria que, por sua forma especial, se presta a um determinado uso.
III. Objeto (estátua de mármore): porção limitada de matéria.
Assinale:
se somente a afirmativa I é correta
se somente a afirmativa II é correta
se somente a afirmativa III é correta.
se somente as afirmativas I e II são corretas.
se as afirmativas I, II e III são corretas.
2.
Multiple Choice
Ponto de fusão, densidade e solubilidade são algumas constantes físicas que caracterizam:
mistura homogênea.
apenas substância simples
mistura heterogênea
substância pura
apenas substância composta
3.
Multiple Choice
Misturas azeotrópicas são:
misturas heterogêneas com ponto de fusão constante
misturas homogêneas ou ligas de ponto de fusão constante.
líquidos ou ligas de ponto de fusão constante.
soluções líquidas de ponto de ebulição constante.
líquidos de ponto de ebulição variável.
4.
Multiple Choice
"Oxigênio, essencial nas reações de combustão e ozonio, agente bactericida no tratamento da água e desodorização de ambientes fechados exemplificam o fenômeno chamado de ...(I)... São substâncias ...(II)... formadas por átomos de um mesmo elemento químico com número atômico ...(III)...". Para completar corretamente a afirmação, I, II e III devem ser substituídos, respectivamente, por
alotropia - simples - 8
isobaria - compostas - 16
isomeria - iônicas - 18
isoformismo - moleculares - 18
tautomeria - orgânicas - 32
5.
Multiple Choice
A água destilada é um exemplo de:
substância simples
composto químico
mistura homogênea
elemento químico
mistura heterogênea
6.
Multiple Choice
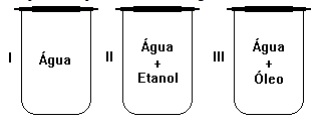
Considerando os sistemas acima, podem ser classificados como:
substância simples, mistura homogênea, mistura heterogênea.
substância composta, mistura heterogênea, mistura heterogênea
substância composta, mistura homogênea, mistura heterogênea.
substância simples, mistura homogênea, mistura homogênea
substância composta, mistura heterogênea, mistura homogênea.

Explore this activity with a free account
Find a similar activity
Create activity tailored to your needs using
.svg)

Equilíbrio Químico
•
University

MODELO ATÔMICO
•
11th - 12th Grade

Substâncias e Misturas
•
1st Grade

Modelos Atômicos
•
8th Grade

Estados da matéria (9°ANO)
•
9th Grade

Grupos Funcionais - Hidrocarboneto e funções oxigenadas (Lição)
•
12th Grade